- HOME
- 医療機器の開発初期段階における安全性規格適合の重要性とは
設計 医療機器ODM
医療機器の開発初期段階における
安全性規格適合の重要性とは
投稿日:
医療機器の開発において、安全性規格への適合は製品化を成功させるための必須要素です。
本記事では、医療機器の開発初期段階で安全性規格を考慮する重要性、具体的な検討ポイント、そして設計仕様にどのように反映させるべきかについて解説します。これにより、効率的な薬機法申請とスムーズな開発プロセスを実現する方法をお伝えします。
目次
医療機器の開発初期で陥りがちな課題
医療機器開発の初期段階では、製品コンセプトや仕様の確立に注力するあまり、安全性規格適合が後回しにされることがあります。しかし、安全性規格への適合は薬機法申請の必須条件であり、これを無視した開発プロセスは後戻りやコスト増につながる可能性があります。
開発初期段階から安全性規格への適合を意識することで、薬機法申請に向けたスムーズなプロセスと、設計品質の向上が期待できます。
医療機器の安全性確保に必要な基本概念
医療機器は単に動作するだけでなく、「安全性」と「有効性」が保証されている必要があります。
これを支えるのが以下の2つの柱です。
- 品質システム:設計から製造、販売後までを通じた一貫した品質保証
- リスクマネジメント:使用時のリスクを評価し、管理する仕組み
これらの柱を支える要素として、以下の3つが重要です。
- 法令・規制:国や地域ごとに定められた遵守すべきルール
- 製品安全規格:製品ごとに必要な安全基準
- 技術水準:現行技術で達成可能な管理基準
これらを基に安全性が確保されます。
医療機器の製品安全性の基本構造
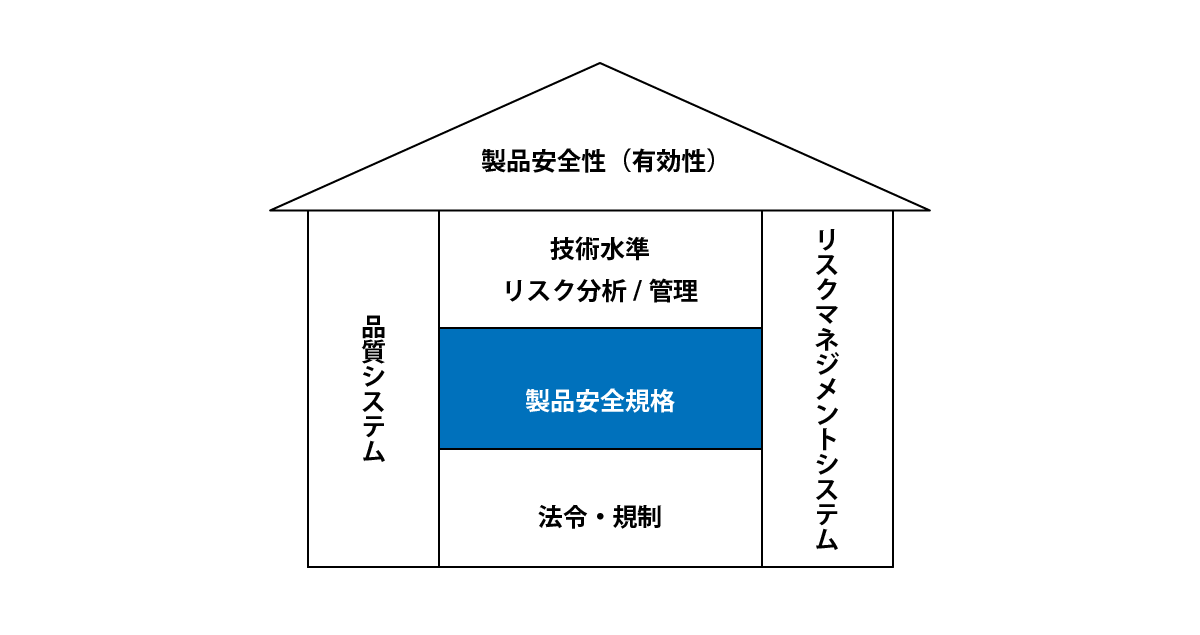
医療機器に求められる安全性規格の種類
特に電気を使用する医療機器(能動医療機器)では、以下の規格に適合する必要があります。
- 通則:基礎的な安全要求事項(例:JIS T 0601-1)
- 副通則:通則に基づき特定の機器に追加される要件
- 個別規格:特定の製品固有の安全性や性能基準
これらを適切に組み合わせて適合することで、安全性を保証します。
以下の図は医療機器の安全設計の一例です。
医療機器の安全設計(CTの例) JIS T 1497、JIS Q 13485
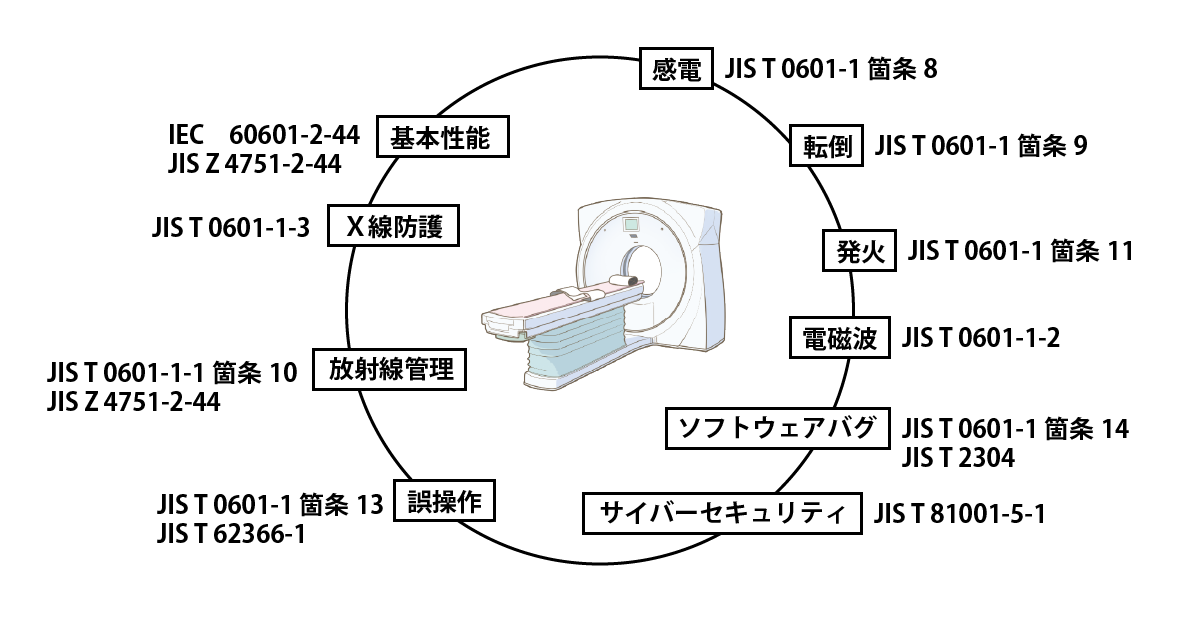
- 感電:JIS T 0601-1 箇条8
- 転倒:JIS T 0601-1 箇条9
- 発火:JIS T 0601-1 箇条11
- 電磁波:JIS T 0601-1-2
- ソフトウェアバグ:JIS T 0601-1箇条14、
JIS T 2304
- サイバーセキュリティ:JIS T 81001-5-1
- 誤操作:JIS T 0601-1箇条13、JIS T 62366-1
- 放射線管理:JIS T 0601-1-1 箇条10、
JIS Z 4751-2-44 - X線防護:JIS T 0601-1-3
- 基本性能:IEC 60601-2-44、JIS Z 4751-2-44
開発初期段階で安全性規格を考慮する必要性
設計初期から安全性規格を仕様に反映させることは、後戻りを防ぐだけでなく、薬機法申請をスムーズに進める鍵となります。
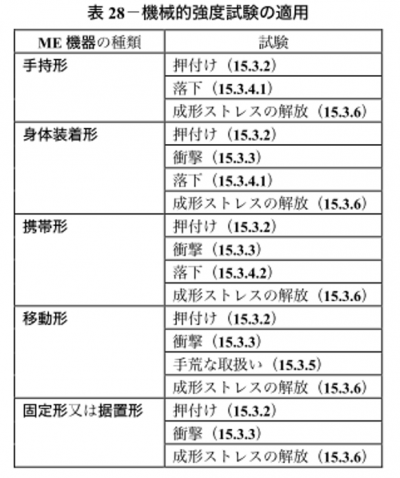
例えば、JIS T 0601-1における機械的強度試験では、表28のように医療機器の種類によって求められる基準が異なります。
これらを事前に確認し、設計に反映することで、規格適合のための再設計を防ぎます。
引用元:JIS T 0601-1:2023 箇条15.3.1 表28
規格適合のためのポイント
適合規格を選択する際には、以下の視点を考慮する必要があります。
- 製品が該当する薬機法や認証基準で求められる規格は何か?
- 製品の性能や安全性に応じて必要な規格はどれか?
- 医療機関や家庭環境など、使用環境に適合した規格は何か?
- 医療従事者が使用するのか、一般消費者が使用するのか?
単に「この規格に適合すればよい」という発想ではなく、製品の特性や使用条件に基づき、安全性規格を初期段階で選択し、設計仕様に反映することが重要です。
医療機器開発の成功につなげるために
医療機器の安全性規格適合は、単なる形式的な要件ではなく、製品の品質を担保し、スムーズな薬機法申請を可能にするための重要なプロセスです。開発初期段階から安全性規格を考慮し、設計に反映することで、効率的かつ高品質な医療機器開発を実現できます。
東京エレクトロンデバイスでは、医療機器開発における要件定義やリスクマネジメントなどのQMS関連の対応も可能ですので、設計の前段階からお客様の製品開発をご支援します。